The relationship between ventricular arrhythmia and myocardial characteristics in magnetic resonance imaging in patients with dilated cardiomyopathy
-
摘要: 目的 探究非缺血性扩张型心肌病(NIDCM)患者磁共振下心肌强化特征与发生室性心律失常(VA)事件的关系,找出相关危险因素。方法 将2019年11月—2021年7月于郑州大学第一附属医院就诊的154例NIDCM患者纳入研究。根据发生VA事件的情况将其分为对照组及失常组,比较两组患者的一般资料及心脏磁共振延迟强化(LGE-CMR)下心肌特征。通过logistic回归分析相关危险因素,并应用受试者工作特征(ROC)曲线分析危险因素的诊断价值。结果 失常组的左室心肌质量(LVM)低于对照组,而年龄、左室舒张末期容积(EDV)、收缩末期容积(ESV)和胺碘酮的应用人数高于对照组(P< 0.05)。LGE-CMR下失常组心肌的灰色区占比高于对照组(P< 0.05),灰色区体积、强化区体积及占比无明显差异。logistic回归提示灰色区占比增加、年龄增大及ESV增大是发生VA的危险因素,而高LVM则为保护因素(P< 0.05)。其中灰色区占比、年龄及LVM诊断VA的曲线下面积(AUC)分别为0.662、0.646和0.607。结论 年龄和灰色区占比增大是NIDCM患者发生VA的独立危险因素,而较高的LVM起保护作用。
-
关键词:
- 室性心律失常 /
- 心脏磁共振 /
- 非缺血性扩张型心肌病 /
- 灰色区
Abstract: Objective The study was performed to explore the relationship between the characteristics of myocardial enhancement and ventricular arrhythmia(VA) in patients with non-ischemic dilated cardiomyopathy(NIDCM) by using magnetic resonance imaging, and identify relevant risk factors.Methods A total of 154 NIDCM patients in the First Affiliated Hospital of Zhengzhou University from November 2019 to July 2021 were enrolled. The patients were divided into control and arrythmia groups based on the occurrence of VA events. The basic data and myocardial characteristics in late gadolinium-enhanced cardiac magnetic resonance(LGE-CMR) of the two groups were compared. The risk factors were analyzed by logistic regression and used to analyze the diagnostic value by ROC curve.Results The left ventricular mass(LVM) in the control group was higher than that in the arrythmia group, but the age, left ventricular end diastolic volume(EDV), end systolic volume(ESV) and number of amiodarone users were lower than those in the arrythmia group(P< 0.05). Using the LGE-CMR, the proportion of gray zone in the control group was lower than that in the arrythmia group(P< 0.05), and there was no significant difference in the volume of gray zone, the volume and proportion of enhancement area(P>0.05). Logistic regression showed that the increase of age, ESV and proportion of gray zone were the risk factors of VA, while the high LVM was the protective factor. And the area under curve(AUC) of proportion of gray zone, age and LVM in VA diagnosis were 0.662, 0.646 and 0.607 respectively.Conclusion The increase in age and the proportion of gray zone are independent risk factors for VA in NIDCM patients, and higher LVM plays a protective role. -
非缺血性扩张型心肌病(NIDCM)是一种以心室扩大及心肌收缩功能降低为主的异质性心肌病[1]。该病由于继发的进展性心力衰竭及心源性猝死有着很高的病死率,在接受治疗情况下5年病死率为20%[2],其中心源性猝死多是由于严重室性心律失常(VA)所致。目前对于NIDCM的危险性分级主要根据左室射血分数(EF),然而部分患者的EF值与面临的猝死风险并不相符,通过心脏磁共振延迟成像(LGE-CMR)技术分析心肌强化区域可以有效帮助预测心律失常等不良事件的发生[3-5]。而灰色区作为强化区域的一部分,因其无序混杂的组成成分,是VA发生的基础[6-7]。本文旨在通过研究LGE-CMR下NIDCM患者的心肌特征,分析发生VA事件相关危险因素,为防治提供理论依据。
1. 对象与方法
1.1 对象
收集2019年11月—2021年7月于郑州大学第一附属医院住院的共计236例符合NIDCM诊断的患者,根据纳入与排除标准,最终选取154例患者纳入研究,结合动态心电图检查结果,将其分成对照组(正常或偶发室性期前收缩 < 500/24 h)66例与失常组(频发室性期前收缩>500/24 h或室性心动过速)88例[8]。
入选标准:①纳入患者需符合NIDCM诊断标准;②需有完善的磁共振报告及影像,同时期动态心电图等资料。
排除标准:①排除关键资料如磁共振及动态心电图等检查缺失的患者;②根据磁共振影像资料,排除图像伪影严重影响心室划分、正常心肌区域选定和后续识别的患者;③排除心脏瓣膜病、缺血性心脏病、高血压病性心脏病、先天性心脏病等继发引起心脏扩大疾病的患者。
本研究符合2013年发布的《赫尔辛基宣言》中涉及人体受试者的医学研究伦理原则。
1.2 基本指标收集
根据患者入院病历资料获得患者的姓名、性别、年龄、身高、体重、糖尿病史、吸烟史、饮酒史及患者目前用药相关情况。患者入院第2日清晨晨起空腹状态下采集外周静脉血,利用全自动生化分析仪检验,收集患者的糖化血红蛋白(HbA1c)、甘油三酯(TG)、总胆固醇(TC)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)、血红蛋白(Hb)、血钾(K)、血钠(Na)、血钙(Ca)、血肌酐(SCr)、血尿酸(UA)、总胆红素(TBil)、白蛋白(ALB)、N端脑钠肽前体(NT-proBNP)、肾小球滤过率(GFR)。同时根据患者入院后完善的磁共振检查结果,获得患者现阶段的左室EF、舒张末期容积(EDV)、收缩末期容积(ESV)、每搏输出量(SV)、心输出量(CO)和左室心肌质量(LVM)。
1.3 磁共振数据处理
磁共振设备与扫描参数:图像采集使用Siemens Skyra 3.0T MR成像仪,18通道表面相控阵线圈,TrueFisp电影序列扫描左心长轴(二、三、四腔心)截面及短轴逐层扫描,TR 38.8 ms,TE 1.4 ms,翻转角80°,层厚8 mm;延迟增强扫描采用Gd-DTPA对比剂,采用高压注射器通过肘静脉推注,流率3 mL/s,后跟注20 mL 0.9%氯化钠,采用相位敏感翻转恢复(PSIR)序列,于对比剂注入10 min后开始LGE-CMR成像,逐层采集短轴层面,TR 657.0 ms,TE 2.0 ms,翻转角20°,层厚8 mm。
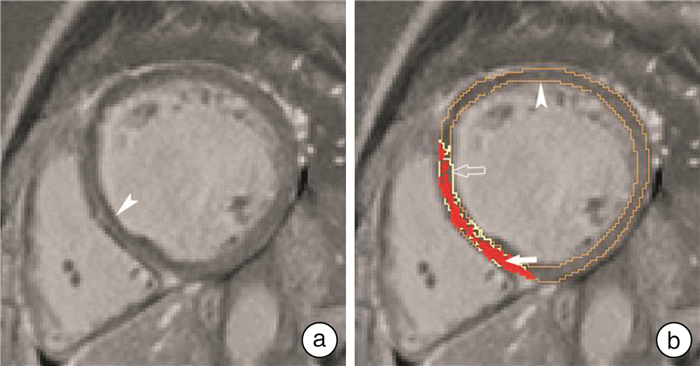
磁共振数据处理与收集:收集患者磁共振图像中PSIR序列的短轴层面,将其导入图像处理软件Seg3D软件(National Institutes of Health Center,USA)[9],在软件中人工勾画心内膜及心外膜(不包括腱索及乳头肌),确定左室心肌范围。在勾画范围内,选取远离延迟强化区的未表现延迟强化的正常心肌作为感兴趣区,利用Fiji软件(National Institute of Mental Health,Bethesda,USA)[10],获得该范围正常心肌信号强度的均值(mean)及标准差(SD),利用正常心肌信号标准差法(signal threshold versus reference mean,STRM),将勾画范围内心肌信号大于mean+3SD的区域定义为强化区,而其中大于mean+5SD的区域为强化核心区,其余区域定义为灰色区[11](见图 1),将对应阈值代入Seg3D软件中由软件自动计算得出对应的强化区域及其中灰色区体积。计算得到强化区占左室心肌体积比值和灰色区占强化区比值。该过程由两名有经验的医师分别独立处理,意见不同经讨论后达成一致。
1.4 统计学处理
收集到的数据通过SPSS 21.0统计软件进行处理,正态分布的计量资料以X±S表示,两组间比较采用t检验;不符合正态分布的计量资料以M(P25,P75)表示,两组间比较采用Mann-Whitney U检验;计数资料以例(%)表示,两组间比较采用χ2检验。利用多因素logistic回归分析NIDCM患者VA的危险因素。并对相关指标的诊断价值采用受试者工作特征(ROC)曲线及曲线下面积(AUC)进行计算。
2. 结果
2.1 一般资料比较
两组患者在性别、身高、体重、糖尿病史、吸烟及饮酒史、HbA1c、TG、TC、HDL-C、LDL-C、Hb、K、Na、Ca、SCr、UA、TBIL、ALB、NT-proBNP、GFR方面无统计学差异。两组患者应用β受体阻滞剂、螺内酯、呋塞米、地高辛、ACEI/ARB、他汀类药物情况无明显差异。失常组的年龄及胺碘酮应用人数高于对照组,差异具有统计学意义(P < 0.05)。见表 1。
表 1 两组患者一般资料比较Table 1 Comparison of basic data between the two groupsX±S, M(P25, P75) 项目 对照组(66例) 失常组(88例) t/Z/χ2值 P值 男/例(%) 53(80.30) 65(73.86) 0.873 0.350 年龄/岁 47.56±13.98 54.16±11.19 -3.151 0.002 身高/cm 171.92±9.35 170.53±7.68 0.809 0.421 体重/kg 76.20±17.11 73.01±13.50 1.227 0.222 糖尿病史/例(%) 8(12.12) 8(9.10) 0.372 0.542 吸烟史/例(%) 25(37.88) 30(34.10) 0.236 0.627 饮酒史/例(%) 20(30.30) 28(31.82) 0.040 0.841 HbA1c/% 5.81(5.60,6.33) 6.0(5.64,6.50) -1.108 0.268 TC/(mmol·L-1) 4.04±0.87 3.80±0.90 1.621 0.107 TG/(mmol·L-1) 1.21(0.87,1.84) 1.17(0.89,1.55) -0.900 0.368 HDL-C/(mmol·L-1) 0.99(0.83,1.17) 1.00(0.82,1.20) -0.210 0.834 LDL-C/(mmol·L-1) 2.55±0.78 2.41±0.72 1.156 0.250 Hb/(g·L-1) 148.00(133.50,163.50) 142.45(133.25,151.43) -1.864 0.062 K/(mmol·L-1) 4.30±0.51 4.29±0.57 0.113 0.910 Na/(mmol·L-1) 141.00(139.65,143.00) 141.00(139.00,142.80) -1.017 0.309 Ca/(mmol·L-1) 2.31(2.23,2.38) 2.32(2.22,2.36) -0.897 0.369 SCr/(μmol·L-1) 81.50(69.83,94.83) 79.00(67.70,90.00) -0.967 0.334 UA/(μmol·L-1) 379.00(316.50,476.00) 370.00(315.25,464.75) -0.586 0.558 TBil/(μmol·L-1) 12.73(9.53,18.46) 13.06(9.10,19.03) -0.343 0.732 ALB/(g·L-1) 41.00(38.15,44.45) 40.60(38.40,43.60) -0.616 0.538 NT-proBNP/(ng·L-1) 933.70(470.00,2273.75) 1147.00(398.58,3421.00) -1.102 0.270 GFR/[mL·min-1·(1.73m2)-1] 92.80(76.79,104.18) 90.76(76.82,101.07) -1.080 0.280 药物应用情况/例(%) β受体阻滞剂 59(89.40) 80(90.91) 0.098 0.754 螺内酯 62(93.94) 81(92.05) 0.204 0.652 呋塞米 54(81.82) 70(79.55) 0.124 0.725 ACEI/ARB类 59(89.40) 84(95.45) 2.089 0.148 他汀类 34(51.52) 38(43.18) 1.052 0.305 地高辛 23(34.85) 28(31.82) 0.156 0.693 胺碘酮 4(6.06) 20(22.73) 7.963 0.005 ACEI/ARB:血管紧张素转化酶抑制剂/血管紧张素受体拮抗剂 2.2 磁共振下心肌特征比较
两组间EF、SV和CO无统计学差异。对照组LVM高于失常组,而EDV、ESV低于失常组,差异有统计学意义(P < 0.05)。两组中均有少量患者磁共振图像未见强化,无统计学差异。对照组灰色区占比低于失常组(P < 0.05),两组间强化区体积及占比、灰色区体积无统计学差异。见表 2。
表 2 比较两组间磁共振下心肌特征Table 2 Evaluating the myocardial characteristics between two groups by using CMRX±S 项目 对照组(66例) 失常组(88例) t/χ2值 P值 EF/% 26.90±9.74 24.58±10.62 1.390 0.166 EDV/mL 273.86±107.19 327.80±192.85 -2.200 0.029 ESV/mL 204.99±95.63 255.86±168.16 -2.363 0.019 SV/mL 71.29±23.41 72.04±35.89 -0.143 0.887 CO/(L·min-1) 5.37±2.08 5.48±3.14 -0.232 0.817 LVM/g 190.76±62.84 171.48±49.21 2.029 0.044 无强化图像数/例(%) 9(13.64) 12(13.64) 0.000 1.000 灰色区体积/cm3 8.37±6.76 9.76±5.79 -1.272 0.206 灰色区占比/% 34.54±12.63 42.81±15.48 -3.292 0.001 总强化区体积/cm3 24.62±16.49 24.62±15.59 -0.002 0.999 总强化区占比/% 16.76±9.08 19.27±11.54 -1.360 0.176 2.3 NIDCM患者VA风险的多因素logistic回归分析
将单变量分析所得差异数据(P < 0.05)纳入模型进行多因素logistic回归分析。结果提示NIDCM患者高灰色区占比、年龄增加及ESV增大是发生VA的危险因素,而高LVM则为保护因素。见表 3。
表 3 NIDCM患者VA风险因素的多因素logistic回归分析Table 3 Multivariate logistic regression results of VA risk factors for NIDCM patients变量 β SE OR 95%CI P值 年龄 0.036 0.017 1.036 1.003~1.070 0.031 ESV 0.011 0.003 1.011 1.005~1.017 0.001 LVM -0.018 0.006 0.982 0.971~0.993 0.002 灰色区占比 0.039 0.017 1.039 1.006~1.073 0.019 常量 -2.123 1.346 0.120 2.4 NIDCM患者VA风险因素的ROC曲线
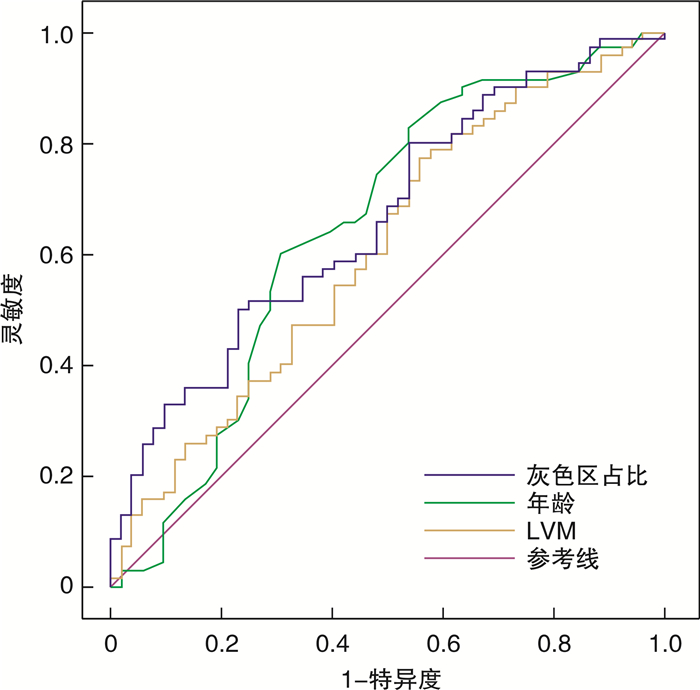
根据多因素logistic回归分析所得风险因素绘制ROC曲线显示,灰色区占比、年龄及LVM的AUC分别为0.662(95%CI 0.565~0.758,P=0.002)、0.646(95%CI 0.543~0.750,P=0.006)和0.607(95%CI 0.505~0.709,P=0.043),ESV的AUC无统计学意义。灰色区占比的最佳截断值为42.80%,敏感度及特异度为50.0%和76.9%;年龄的最佳截断值为53.5岁,敏感度及特异度为60.0%和69.2%;LVM的最佳截断值为204.2 g,敏感度及特异度为77.1%和44.2%。见图 2。
3. 讨论
NIDCM患者在多种病因影响下,心肌细胞受损死亡伴随细胞外基质纤维蛋白沉积,导致原有正常心肌逐渐被纤维组织替代,心肌顺应性降低,心室扩大和收缩功能减退[12-13]。并会影响心肌细胞正常电生理功能,出现严重VA事件造成猝死等恶性后果[14-15]。本研究发现年龄增加、ESV增大及LVM减少为VA的危险因素,这与心肌损伤长时间积累导致心室扩大、室壁变薄及心脏收缩能力减弱有关。
目前常用于评估NIDCM患者预后的EF值被指与风险不符,大约48%的患者遭受心源性猝死但EF值正常[3, 16]。有研究指出,评估心肌纤维化程度在预测恶性VA上的作用不可忽视,LGE-CMR下患者肌壁间强化与心律失常有很强的相关性[3]。Mandawat等[17]在长期随访中发现18%的NIDCM患者心肌纤维化进展,这与左室持续重构有关且会增大患者的死亡风险,剩余患者心肌纤维化程度未有变化。因此可将其作为一种稳定的指标在LGE-CMR下分析特征评估患者发生VA的风险[18]。我们发现两组中均有少量患者LGE-CMR未见明显强化,这与LGE-CMR图像分辨率限制,无法有效识别弥漫性显微下间质纤维化有关[19]。所以对于无强化患者,不可忽视其VA风险。
已有研究报道VA多发生于LGE-CMR影像中心肌强化的灰色区域,因其处于纤维组织与正常心肌的交界处,在图像上呈灰色而得名。在这一区域内存活与死亡的心肌组织无序混杂,残存心肌细胞线粒体功能障碍,纤维组织增生替代凋亡心肌,心肌间连接异常,这些结构及功能异常使得心肌细胞间电传导缓慢或阻滞,易形成折返通路继而导致严重VA事件发生[18, 20]。Chen等[21]指出灰色区与VA独立相关,有预测非缺血性心肌病患者心律失常的潜力。这些区域存在电生理异常,为持续性室性心动过速的起始点[22]。本研究发现,在两组患者心肌总强化体积及占比无明显差异情况下,失常组患者心肌的灰色区占比要高于对照组[(42.81%±15.48%)∶(34.54%±12.63%),P < 0.05],logistic回归显示灰色区占比增大是NIDCM患者出现VA的危险因素。考虑到灰色区在VA的发生和维持中起重要作用,而且消融后残留的灰色区也被认为可能是临床复发的基础[23-24],所以下一步对其继续研究能为相关事件的防治提供依据。
综上所述,利用LGE-CMR技术评估患者心肌特征,通过研究灰色区占比相关数据,有助于评估严重VA事件风险,也可为治疗提供理论依据。同时,年龄及LVM也与VA风险有关。本研究也存在一定局限性:①纳入样本量较少,单中心研究缺乏长期随访资料;②本文中用到的图像分析方法易受图像质量干扰,影响阈值识别准确性。
利益冲突 所有作者均声明不存在利益冲突
-
表 1 两组患者一般资料比较
Table 1. Comparison of basic data between the two groups
X±S, M(P25, P75) 项目 对照组(66例) 失常组(88例) t/Z/χ2值 P值 男/例(%) 53(80.30) 65(73.86) 0.873 0.350 年龄/岁 47.56±13.98 54.16±11.19 -3.151 0.002 身高/cm 171.92±9.35 170.53±7.68 0.809 0.421 体重/kg 76.20±17.11 73.01±13.50 1.227 0.222 糖尿病史/例(%) 8(12.12) 8(9.10) 0.372 0.542 吸烟史/例(%) 25(37.88) 30(34.10) 0.236 0.627 饮酒史/例(%) 20(30.30) 28(31.82) 0.040 0.841 HbA1c/% 5.81(5.60,6.33) 6.0(5.64,6.50) -1.108 0.268 TC/(mmol·L-1) 4.04±0.87 3.80±0.90 1.621 0.107 TG/(mmol·L-1) 1.21(0.87,1.84) 1.17(0.89,1.55) -0.900 0.368 HDL-C/(mmol·L-1) 0.99(0.83,1.17) 1.00(0.82,1.20) -0.210 0.834 LDL-C/(mmol·L-1) 2.55±0.78 2.41±0.72 1.156 0.250 Hb/(g·L-1) 148.00(133.50,163.50) 142.45(133.25,151.43) -1.864 0.062 K/(mmol·L-1) 4.30±0.51 4.29±0.57 0.113 0.910 Na/(mmol·L-1) 141.00(139.65,143.00) 141.00(139.00,142.80) -1.017 0.309 Ca/(mmol·L-1) 2.31(2.23,2.38) 2.32(2.22,2.36) -0.897 0.369 SCr/(μmol·L-1) 81.50(69.83,94.83) 79.00(67.70,90.00) -0.967 0.334 UA/(μmol·L-1) 379.00(316.50,476.00) 370.00(315.25,464.75) -0.586 0.558 TBil/(μmol·L-1) 12.73(9.53,18.46) 13.06(9.10,19.03) -0.343 0.732 ALB/(g·L-1) 41.00(38.15,44.45) 40.60(38.40,43.60) -0.616 0.538 NT-proBNP/(ng·L-1) 933.70(470.00,2273.75) 1147.00(398.58,3421.00) -1.102 0.270 GFR/[mL·min-1·(1.73m2)-1] 92.80(76.79,104.18) 90.76(76.82,101.07) -1.080 0.280 药物应用情况/例(%) β受体阻滞剂 59(89.40) 80(90.91) 0.098 0.754 螺内酯 62(93.94) 81(92.05) 0.204 0.652 呋塞米 54(81.82) 70(79.55) 0.124 0.725 ACEI/ARB类 59(89.40) 84(95.45) 2.089 0.148 他汀类 34(51.52) 38(43.18) 1.052 0.305 地高辛 23(34.85) 28(31.82) 0.156 0.693 胺碘酮 4(6.06) 20(22.73) 7.963 0.005 ACEI/ARB:血管紧张素转化酶抑制剂/血管紧张素受体拮抗剂 表 2 比较两组间磁共振下心肌特征
Table 2. Evaluating the myocardial characteristics between two groups by using CMR
X±S 项目 对照组(66例) 失常组(88例) t/χ2值 P值 EF/% 26.90±9.74 24.58±10.62 1.390 0.166 EDV/mL 273.86±107.19 327.80±192.85 -2.200 0.029 ESV/mL 204.99±95.63 255.86±168.16 -2.363 0.019 SV/mL 71.29±23.41 72.04±35.89 -0.143 0.887 CO/(L·min-1) 5.37±2.08 5.48±3.14 -0.232 0.817 LVM/g 190.76±62.84 171.48±49.21 2.029 0.044 无强化图像数/例(%) 9(13.64) 12(13.64) 0.000 1.000 灰色区体积/cm3 8.37±6.76 9.76±5.79 -1.272 0.206 灰色区占比/% 34.54±12.63 42.81±15.48 -3.292 0.001 总强化区体积/cm3 24.62±16.49 24.62±15.59 -0.002 0.999 总强化区占比/% 16.76±9.08 19.27±11.54 -1.360 0.176 表 3 NIDCM患者VA风险因素的多因素logistic回归分析
Table 3. Multivariate logistic regression results of VA risk factors for NIDCM patients
变量 β SE OR 95%CI P值 年龄 0.036 0.017 1.036 1.003~1.070 0.031 ESV 0.011 0.003 1.011 1.005~1.017 0.001 LVM -0.018 0.006 0.982 0.971~0.993 0.002 灰色区占比 0.039 0.017 1.039 1.006~1.073 0.019 常量 -2.123 1.346 0.120 -
[1] 中华医学会心血管病学分会, 中国心肌炎心肌病协作组. 中国扩张型心肌病诊断和治疗指南[J]. 临床心血管病杂志, 2018, 34(5): 421-434.
[2] Felker GM, Thompson RE, Hare JM, et al. Underlying causes and long-term survival in patients with initially unexplained cardiomyopathy[J]. N Engl J Med, 2000, 342(15): 1077-1084. doi: 10.1056/NEJM200004133421502
[3] Gulati A, Jabbour A, Ismail TF, et al. Association of fibrosis with mortality and sudden cardiac death in patients with nonischemic dilated cardiomyopathy[J]. JAMA, 2013, 309(9): 896-908. doi: 10.1001/jama.2013.1363
[4] Nelson T, Garg P, Clayton RH, et al. The Role of cardiac MRI in the management of ventricular arrhythmias in ischaemic and non-ischaemic dilated cardiomyopathy[J]. Arrhythm Electrophysiol Rev, 2019, 8(3): 191-201. doi: 10.15420/aer.2019.5.1
[5] Shenasa M. Fibrosis and ventricular arrhythmogenesis: role of cardiac MRI[J]. Card Electrophysiol Clin, 2019, 11(3): 551-562. doi: 10.1016/j.ccep.2019.06.002
[6] Disertori M, Masè M, Ravelli F. Myocardial fibrosis predicts ventricular tachyarrhythmias[J]. Trends Cardiovasc Med, 2017, 27(5): 363-372. doi: 10.1016/j.tcm.2017.01.011
[7] 王璐静, 姜安谧, 金富伟, 等. CMR量化评价心肌梗死周围边缘带预测室性心律失常的研究进展[J]. 临床心血管病杂志, 2021, 37(6): 585-588. https://www.cnki.com.cn/Article/CJFDTOTAL-LCXB202106019.htm
[8] 中华医学会心电生理和起搏分会, 中国医师协会心律学专业委员会. 2020室性心律失常中国专家共识(2016共识升级版)[J]. 中华心律失常学杂志, 2020, 24(3): 111-115. https://www.cnki.com.cn/Article/CJFDTOTAL-ZGXZ202003002.htm
[9] Institute SCaI. "Seg3D" Volumetric Image Segmentation and Visualization. Scientific Computing and Imaging Institute(SCI). Available at: http://www.seg3d.org.
[10] Schindelin J, Arganda-Carreras I, Frise E, et al. An open-source platform for biological-image analysis[J]. Nat Methods, 2012, 9(7): 676-682. doi: 10.1038/nmeth.2019
[11] Gouda S, Abdelwahab A, Salem M, et al. Scar characteristics for prediction of ventricular arrhythmia in ischemic cardiomyopathy[J]. Pacing Clin Electrophysiol, 2015, 38(3): 311-318. doi: 10.1111/pace.12536
[12] Schultheiss HP, Fairweather D, Caforio A, et al. Dilated cardiomyopathy[J]. Nat Rev Dis Primers, 2019, 5(1): 32. doi: 10.1038/s41572-019-0084-1
[13] Becker M, Cornel JH, van de Ven PM, et al. The Prognostic value of late gadolinium-enhanced cardiac magnetic resonance imaging in nonischemic dilated cardiomyopathy: a review and meta-analysis[J]. JACC Cardiovasc Imaging, 2018, 11(9): 1274-1284. doi: 10.1016/j.jcmg.2018.03.006
[14] Willis MS, Yates CC, Schisler JC. Fibrosis in Disease: An Organ-Based Guide to Disease Pathophysiology and Therapeutic Considerations[J]. Springer, 2018: 111.
[15] Berruezo A, Jáuregui B, Penela D. Towards an improved and personalized risk stratification of sudden cardiac death in dilated non-ischaemic cardiomyopathy: is the time for ejection fraction coming to an end?[J]. Eur Heart J Cardiovasc Imaging, 2021, 22(10): 1139-1141. doi: 10.1093/ehjci/jeab147
[16] Stecker EC, Vickers C, Waltz J, et al. Population-based analysis of sudden cardiac death with and without left ventricular systolic dysfunction[J]. JACC, 2006, 47(6): 1161-1166. doi: 10.1016/j.jacc.2005.11.045
[17] Mandawat A, Chattranukulchai P, Mandawat A, et al. Progression of myocardial fibrosis in nonischemic DCM and association with mortality and heart failure outcomes[J]. JACC Cardiovasc Imaging, 2021, 14(7): 1338-1350. doi: 10.1016/j.jcmg.2020.11.006
[18] Centurión OA, Alderete JF, Torales JM, et al. Myocardial fibrosis as a pathway of prediction of ventricular arrhythmias and sudden cardiac death in patients with nonischemic dilated cardiomyopathy[J]. Crit Pathw Cardiol, 2019, 18(2): 89-97. doi: 10.1097/HPC.0000000000000171
[19] Barison A, Grigoratos C, Todiere G, et al. Myocardial interstitial remodelling in non-ischaemic dilated cardiomyopathy: insights from cardiovascular magnetic resonance[J]. Heart Fail Rev, 2015, 20(6): 731-749. doi: 10.1007/s10741-015-9509-4
[20] Balaban G, Halliday BP, Bai W, et al. Scar shape analysis and simulated electrical instabilities in a non-ischemic dilated cardiomyopathy patient cohort[J]. PLoS Comput Biol, 2019, 15(10): e1007421. doi: 10.1371/journal.pcbi.1007421
[21] Chen Z, Sohal M, Voigt T, et al. Myocardial tissue characterization by cardiac magnetic resonance imaging using T1 mapping predicts ventricular arrhythmia in ischemic and non-ischemic cardiomyopathy patients with implantable cardioverter-defibrillators[J]. Heart Rhythm, 2015, 12(4): 792-801. doi: 10.1016/j.hrthm.2014.12.020
[22] Pham VT, Lin C, Tran TT, et al. Predicting ventricular tachyarrhythmia in patients with systolic heart failure based on texture features of the gray zone from contrast-enhanced magnetic resonance imaging[J]. J Cardiol, 2020, 76(6): 601-609. doi: 10.1016/j.jjcc.2020.06.020
[23] Estner HL, Zviman MM, Herzka D, et al. The critical isthmus sites of ischemic ventricular tachycardia are in zones of tissue heterogeneity, visualized by magnetic resonance imaging[J]. Heart Rhythm, 2011, 8(12): 1942-1949. doi: 10.1016/j.hrthm.2011.07.027
[24] Oduneye SO, Pop M, Shurrab M, et al. Distribution of abnormal potentials in chronic myocardial infarction using a real time magnetic resonance guided electrophysiology system[J]. Journal of cardiovascular magnetic resonance, 2015, 17(1): 27. doi: 10.1186/s12968-015-0133-1
期刊类型引用(6)
1. 赵杨,梁晟昊. 磁共振成像与超声心动图检查在扩张型心肌病诊断中的对比研究. 中华解剖与临床杂志. 2024(02): 124-127 .  百度学术
百度学术
2. 周宇璇,李三军,周云英,邵靓,金佳俊. 基于虚拟现实技术的中医传统功法对扩张型心肌病患者心功能及生活质量影响的研究. 中国医学创新. 2024(06): 90-94 .  百度学术
百度学术
3. 刘娜. 扩张型心肌病患者发生室性心律失常的影响因素. 中国民康医学. 2023(08): 4-6+10 .  百度学术
百度学术
4. 李琰,郭洋洋,赵森,杜森,周青. CT评估老年缺血性心肌病心衰患者EAT、PCAT水平变化及与血清NT-proBNP、Gal-3表达的相关性. 中国医学工程. 2023(10): 19-23 .  百度学术
百度学术
5. 高雨洁,徐怡,廖深根,钱雯,祝因苏,李新立. 非缺血性扩张型心肌病患者NT-proBNP与心脏磁共振初始T1值的相关性. 中国医学影像学杂志. 2022(07): 669-675 .  百度学术
百度学术
6. 张国新. 美托洛尔联合胺碘酮治疗冠心病合并室性心律失常的临床疗效及安全性分析. 吉林医学. 2022(10): 2748-2750 .  百度学术
百度学术
其他类型引用(2)
-
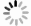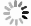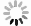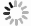



 下载:
下载: